Gobierno de Petro avanza en licencia obligatoria para medicamentos contra hepatitis C
El Gobierno del presidente Gustavo Petro ha dado un paso crucial para cerrar un proceso que lleva más de una década abierto, relacionado con el acceso a tratamientos para la hepatitis C. A través de la resolución 453 de 2026, el Ministerio de Salud, bajo la dirección de Guillermo Alfonso Jaramillo, ha declarado que existen razones de interés público para aplicar una licencia obligatoria sobre las patentes de los Antivirales de Acción Directa (AAD) contra esta enfermedad.
En términos prácticos, esta medida permitiría que otros fabricantes produzcan versiones genéricas de estos medicamentos y las comercialicen en Colombia, siguiendo un mecanismo similar al utilizado recientemente con el Dolutegravir. Sin embargo, el proceso para la hepatitis C tiene una historia mucho más extensa, que se remonta a octubre de 2015, cuando la Fundación IFARMA presentó la solicitud inicial ante el Ministerio de Salud.
Un largo camino hacia la decisión
Durante los años siguientes, se surtieron diversos procedimientos, incluyendo revisiones técnicas y jurídicas, la participación de comités de expertos, la recolección de pruebas y la intervención de laboratorios farmacéuticos que defendieron la vigencia de sus patentes. En 2017, el Ministerio expidió la resolución 5246, dando inicio formal al trámite administrativo, aunque sin una decisión de fondo en ese momento.
El proceso avanzó lentamente, con análisis y recomendaciones que en ocasiones desaconsejaron la declaratoria, reflejando un debate constante entre el acceso a medicamentos y la protección de la propiedad intelectual. Ese mismo año, Colombia encontró una alternativa para adquirir estos fármacos a un menor costo, comprándolos a la Organización Panamericana de la Salud (OPS), que negocia con laboratorios y los vende a gobiernos de la región.
No obstante, el proceso de licencia obligatoria permaneció congelado hasta ahora. Con la nueva resolución, el Minsalud declara la existencia de razones de interés público, un requisito legal indispensable para que la Superintendencia de Industria y Comercio pueda otorgar las licencias obligatorias.
Cambios significativos en el enfoque
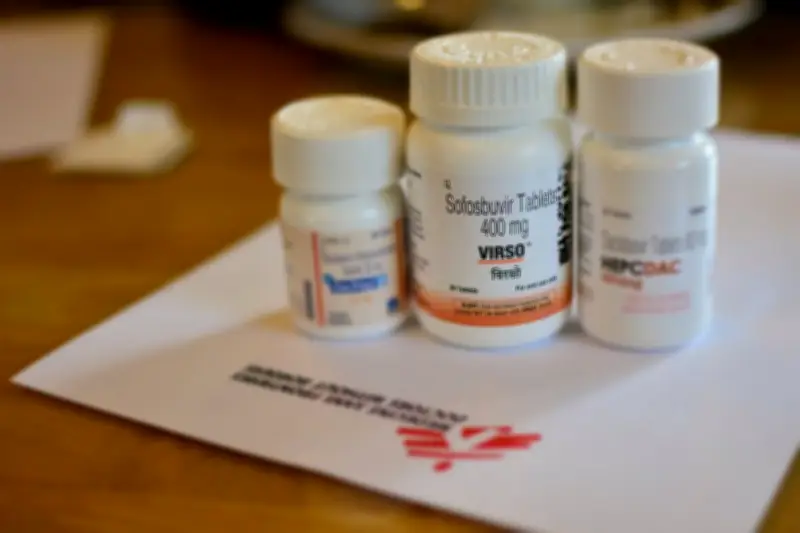
A diferencia de las solicitudes iniciales centradas en moléculas individuales, la resolución 453 se enfoca en combinaciones de Antivirales de Acción Directa (AAD) pangenotípicos de última generación: Sofosbuvir + Velpatasvir y Sofosbuvir + Velpatasvir + Voxilaprevir. Estas combinaciones son más efectivas, con tasas de curación superiores al 95%, y más fáciles de administrar que los esquemas anteriores.
Se incluye además el Voxilaprevir, una molécula esencial para pacientes que han fallado en tratamientos previos y presentan resistencias. Antes de esta resolución, este medicamento se clasificaba como "vital no disponible", lo que generaba barreras y demoras en su acceso, según el documento del Minsalud.
Con estas decisiones, el gobierno estima que, al permitir la entrada de versiones genéricas mediante la licencia obligatoria, el precio por frasco de tratamientos como el Sofosbuvir + Velpatasvir podría reducirse en más de un 90%, pasando de aproximadamente COP 4.095.343 a unos COP 311.908.
Contexto epidemiológico y aumento de casos
El panorama de la hepatitis C en Colombia ha cambiado significativamente en los últimos años, no solo en el número de personas afectadas, sino también en la forma en que el sistema de salud enfrenta la enfermedad. La resolución 453 recoge varias de estas transformaciones, ayudando a entender por qué la decisión se toma en este momento.
Los casos han venido en aumento de manera preocupante. Según la Cuenta de Alto Costo, los casos incidentes pasaron de 314 en 2020 a 1.255 en 2024. A su vez, el Instituto Nacional de Salud reportó un crecimiento de 893 diagnósticos en 2021 a 1.883 en 2024. Solo en el primer semestre de 2025 se registraron 796 diagnósticos, lo que representa un incremento del 46,6% frente al mismo periodo del año anterior.
Detrás de estas cifras, la tasa de incidencia prácticamente se duplicó en pocos años, al pasar de 1,7 casos por cada 100.000 habitantes en 2021 a 3,6 en 2024. Además, ha cambiado la manera de diagnosticar y tratar la enfermedad, con mayor capacidad de detección y nuevas guías que permiten a más médicos iniciar tratamiento, ampliando el acceso pero aumentando la demanda de medicamentos.
Límites del modelo actual y próximos pasos
El modelo basado en compras centralizadas de medicamentos de marca, aunque redujo precios a través de la OPS, empezó a mostrar límites ante el aumento masivo de la demanda proyectada para 2025. El presupuesto disponible podría ser insuficiente para mantener el acceso universal con medicamentos de marca, por lo que el Minsalud insiste en la necesidad de la licencia obligatoria para reducir costos.
Después de la Resolución 453 de 2026, el proceso no ocurre de inmediato. Las farmacéuticas dueñas de las patentes, como Gilead, tienen un plazo de 10 días hábiles para presentar un recurso de reposición. Una vez superado ese punto, el proceso pasa a la Superintendencia de Industria y Comercio, encargada de otorgar las licencias obligatorias que permiten a otros laboratorios producir o importar versiones genéricas.
Cuando la resolución queda ejecutoriada y se publica oficialmente, los fabricantes interesados pueden avanzar en los trámites necesarios para ingresar al mercado, cumpliendo con los requisitos sanitarios revisados por el Invima. Este paso marca un hito en la lucha por el acceso a medicamentos esenciales en Colombia.









